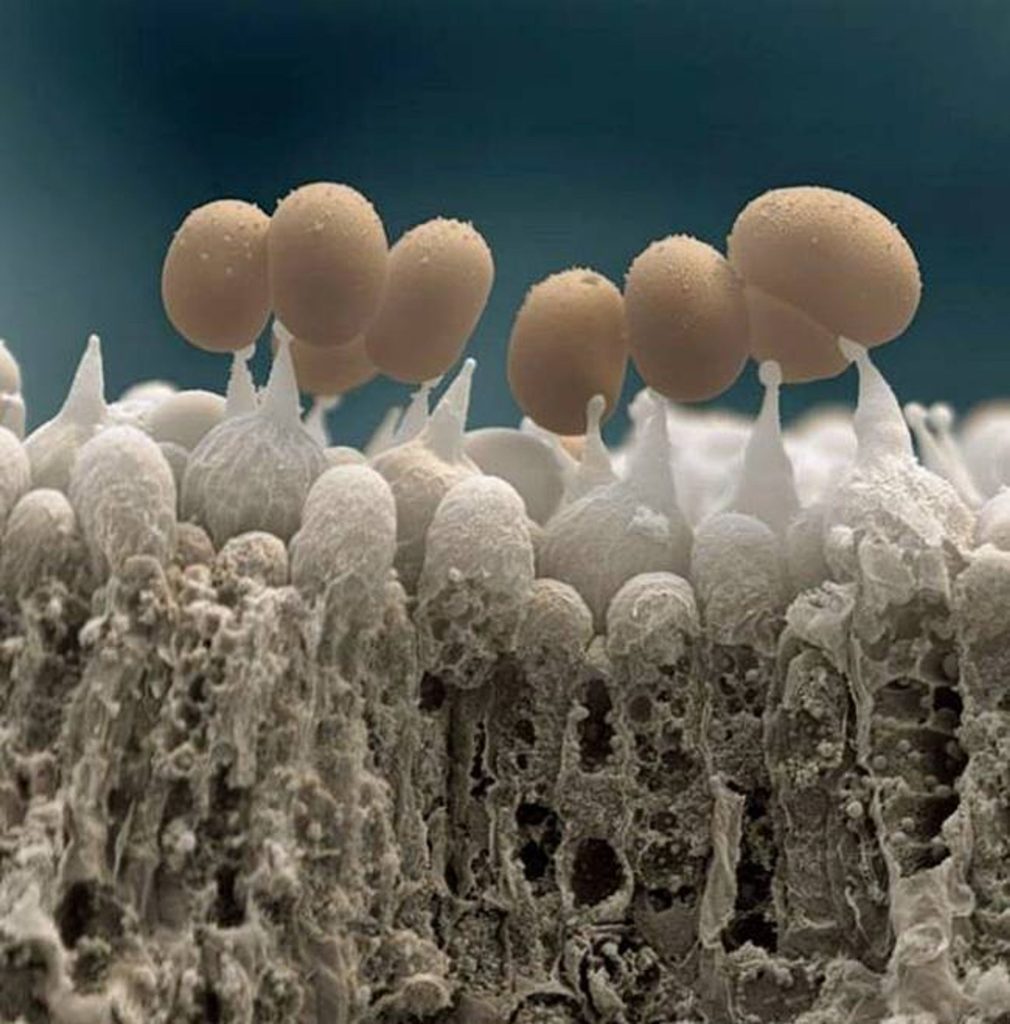
Jmenuje se Aspergillus flavus a je studován na Pensylvánské univerzitě.
Vědci přeměnili molekuly houby Aspergillus flavus, která byla spojována se smrtí při vykopávkách hrobek, jako je hrobka Tutanchamona, na účinnou protinádorovou sloučeninu. (EFE)
Science Editorial – Skupina vědců přeměnila molekuly houby Aspergillus flavus na účinnou protinádorovou látku. Aspergillus flavus je toxická houba, která napadá zemědělské plodiny a je spojována se smrtelnými případy při vykopávkách starověkých hrobek.Co vědci dělají s 4000 gravinami nasbíranými během bouře?K Associated Press
Vědci pod vedením Pensylvánské univerzity ( USA ) modifikovali některé z jeho molekul a otestovali je na buňkách leukémie. Výsledkem je slibná protinádorová sloučenina , která otevírá nové možnosti pro objev dalších léků na bázi hub.

„Houby nám daly penicilin. Nyní nám tyto nové výsledky ukazují, že ještě mnoho léků získaných z přírodních produktů čeká na objevení,“ zdůrazňuje Sherry Gao, profesorka bioinženýrství na Pensylvánské univerzitě a hlavní autorka studie, jejíž podrobnosti byly zveřejněny v pondělí v časopise Nature Chemical Biology.
Aspergillus flavus, pojmenovaný podle svých žlutých spor, byl dlouho považován za zlověstný mikroorganismus. Poté, co archeologové v 20. letech 20. století objevili hrobku Tutanchamona, vedla řada předčasných úmrtí členů týmu provádějícího vykopávky k prokletí faraóna.
O desetiletí později lékaři předpokládali, že určitou roli mohly hrát spóry hub, které spaly po tisíciletí.
A v 70. letech vstoupila do hrobky Kazimíra IV. v Polsku skupina vědců a stalo se to znovu: během několika týdnů jich deset zemřelo. Další výzkumy ukázaly, že v hrobce se nacházel A. flavus, jehož toxiny mohou způsobit plicní infekce.
Nyní se tato houba stala nečekaným zdrojem nové slibné metody léčby rakoviny.
Vzácný nález
Terapie, o které je řeč, představuje třídu modifikovaných ribozomálně syntetizovaných peptidů, neboli RiPP. Název odkazuje na to, jak je sloučenina vyráběna – ribozomem, malou buněčnou strukturou, která produkuje bílkoviny – a na skutečnost, že je následně modifikována, v tomto případě za účelem posílení jejích protinádorových vlastností.
„Tyto chemické látky je obtížné vyčistit ,“ vysvětluje Cyuue Ne , vědecký pracovník z Pensylvánie a první autor článku.
Ačkoli u bakterií byly objeveny tisíce RiPP, u hub jich bylo nalezeno pouze několik.
Aby objevili houbové RiPP, tým nejprve analyzoval tucet kmenů Aspergillus, které podle předchozích studií mohou obsahovat více těchto chemických látek.
Porovnáním chemických látek produkovaných těmito kmeny se známými stavebními bloky RiPP určili vědci A. flavus jako slibného kandidáta pro další studium.
Genetická analýza identifikovala určitý protein v A. flavus jako zdroj houbového RiPP. Když vědci vyřadili geny, které tento protein vytvářejí, chemické markery indikující přítomnost RiPP také zmizely.
Tento nový přístup, který kombinuje metabolické a genetické informace, nejen identifikoval zdroj fungálních RiPP v A. flavus, ale může být také použit k hledání dalších fungálních RiPP v budoucnu.

Silný lék?
Po čištění čtyř různých RiPP vědci zjistili, že molekuly mají jedinečnou strukturu propojených kruhů, kterou nazvali „aspergimyciny“.
I bez úprav prokázaly aspergimyciny při smíchání s lidskými rakovinnými buňkami svůj léčebný potenciál: dvě ze čtyř variant měly silný účinek na leukemické buňky.
Další varianta, ke které vědci přidali lipid obsažený také v mateřském mléce, který vyživuje vyvíjející se včely, se ukázala stejně účinná jako cytarabín a daunorubicin – dva léky schválené zdravotnickými orgány USA a desítky let používané k léčbě leukémie.
V dalších experimentech výzkumníci zjistili, že aspergimyciny pravděpodobně narušují proces dělení buněk.
„Rakovinné buňky se nekontrolovatelně dělí. Tyto sloučeniny blokují tvorbu mikrotubulů, které jsou nezbytné pro dělení buněk “, vysvětluje Gao.
Je pozoruhodné, že tyto sloučeniny neměly žádný nebo jen nepatrný vliv na buňky rakoviny prsu, jater nebo plic , stejně jako na řadu bakterií a plísní, což naznačuje, že destruktivní účinek aspergimycinů je specifický pro určité typy buněk, což je pro jakýkoli budoucí lék velmi důležitá vlastnost.
Kromě prokázání léčebného potenciálu aspergimycinů vědci objevili podobné genové klastry u jiných hub, což naznačuje, že ještě budou objeveny další houbové RiPPS.
Dalším krokem bude testování aspergimycinů na zvířecích modelech s nadějí, že v budoucnu bude možné přejít k klinickým zkouškám na lidech.